தனிமங்களைப் பிரித்தெடுக்கும் முன்னர் இருமல் பற்றிய கருத்தரங்கு பற்றி இங்கே குறிப்பிடுகிறேன். இருமல் பற்றிய கருத்தரங்கு மூன்று தினங்கள் நடந்தது. நூற்றுக்கும் குறைவாகவே கலந்து கொண்டனர். மூன்று நாட்கள் இந்த கருத்தரங்கு நடந்தது.
ஒருவருக்கு இருமல் ஏன் வருகிறது? எதனால் வருகிறது? அதை எப்படி தடுப்பது என்பது குறித்து ஆராய்ச்சிகளைப் பேசினார்கள். இருமல் நமது உடலுக்கு ஒரு தடுப்புச் சாதனம் அதை ஏன் தடுத்து நிறுத்த வேண்டும் என ஒருவர் கேட்டார். இருமல் தடுப்புச் சாதனம்தான் ஆனால் அதுவே ஒருவருக்குத் தொடர்ந்து வரும்போது எவ்வளவு அவதி என்பதை இருமினால்தான் தெரியும் என்றார் அதற்கு பதில் அளித்தவர்.
பேசினால் இருமல் வருகிறது, சிரித்தால் இருமல் வருகிறது, வெயிலில் நின்றால் இருமல் வருகிறது, குளிர் அடித்தால் இருமல் வருகிறது. இப்படி சகலத்துக்கும் இருமல் வருகிறது இதைத் தடுக்க வழி இல்லையா என ஆராய்ச்சியாளர்கள் பேசியதைப் பார்க்கும்போது இன்னும் நிறைய தொலைவு செல்ல வேண்டியிருக்கிறது என்றுதான் பட்டது. ஆனால் இருமல் எதனால் ஏற்படுகிறது என மூளையில் ஏற்படும் மாற்றங்களை படம்பிடித்து போடும் அளவிற்கு ஆராய்ச்சி முன்னேறி இருப்பது வியத்தகு சாதனையே.
மத்திய நரம்பு மண்டலமா, சுற்றியுள்ள நரம்பு மண்டலமா இருமலுக்கு காரணம் எனப் பார்க்கும்போது இரண்டும்தான் என பதில் அளித்தார்கள். பல சுவாரஸ்யமான தகவலுடன் கருத்தரங்கு நடைபெற்றது. இருமலுக்கு என ஒரே ஒரு மருந்துதான் இதுவரை வெளிவந்து உள்ளது. அதுவும் அந்த மருந்து ஒரு செடியிலிருந்து பிரித்தெடுத்து இருக்கிறார்கள். குவெய்ஃபெனசின் என அந்த மருந்தின் பெயர். இதுதான் இருமலுக்கு என அங்கீகரிக்கப்பட்ட மருந்து. மற்றதெல்லாம் அலர்ஜியை கட்டுப்படுத்தக்கூடியவையே. பல மருந்துகள் ஆராய்ச்சிநிலையிலே இன்னும் இருக்கின்றன என்பது வருந்ததக்க விசயம்.
எனது ஆராய்ச்சியை பற்றி எழுதும்போது இது குறித்து மிக விளக்கமாக எழுதுகிறேன். ஏனெனில் நான் முதன்முதலில் எடு்த்துக்கொண்ட ஆராய்ச்சியும் இப்போது செய்து வரும் ஆராய்ச்சிக்கும் அதிக தொடர்பு உண்டு.
ஒருவருக்கு இருமல் ஏன் வருகிறது? எதனால் வருகிறது? அதை எப்படி தடுப்பது என்பது குறித்து ஆராய்ச்சிகளைப் பேசினார்கள். இருமல் நமது உடலுக்கு ஒரு தடுப்புச் சாதனம் அதை ஏன் தடுத்து நிறுத்த வேண்டும் என ஒருவர் கேட்டார். இருமல் தடுப்புச் சாதனம்தான் ஆனால் அதுவே ஒருவருக்குத் தொடர்ந்து வரும்போது எவ்வளவு அவதி என்பதை இருமினால்தான் தெரியும் என்றார் அதற்கு பதில் அளித்தவர்.
பேசினால் இருமல் வருகிறது, சிரித்தால் இருமல் வருகிறது, வெயிலில் நின்றால் இருமல் வருகிறது, குளிர் அடித்தால் இருமல் வருகிறது. இப்படி சகலத்துக்கும் இருமல் வருகிறது இதைத் தடுக்க வழி இல்லையா என ஆராய்ச்சியாளர்கள் பேசியதைப் பார்க்கும்போது இன்னும் நிறைய தொலைவு செல்ல வேண்டியிருக்கிறது என்றுதான் பட்டது. ஆனால் இருமல் எதனால் ஏற்படுகிறது என மூளையில் ஏற்படும் மாற்றங்களை படம்பிடித்து போடும் அளவிற்கு ஆராய்ச்சி முன்னேறி இருப்பது வியத்தகு சாதனையே.
மத்திய நரம்பு மண்டலமா, சுற்றியுள்ள நரம்பு மண்டலமா இருமலுக்கு காரணம் எனப் பார்க்கும்போது இரண்டும்தான் என பதில் அளித்தார்கள். பல சுவாரஸ்யமான தகவலுடன் கருத்தரங்கு நடைபெற்றது. இருமலுக்கு என ஒரே ஒரு மருந்துதான் இதுவரை வெளிவந்து உள்ளது. அதுவும் அந்த மருந்து ஒரு செடியிலிருந்து பிரித்தெடுத்து இருக்கிறார்கள். குவெய்ஃபெனசின் என அந்த மருந்தின் பெயர். இதுதான் இருமலுக்கு என அங்கீகரிக்கப்பட்ட மருந்து. மற்றதெல்லாம் அலர்ஜியை கட்டுப்படுத்தக்கூடியவையே. பல மருந்துகள் ஆராய்ச்சிநிலையிலே இன்னும் இருக்கின்றன என்பது வருந்ததக்க விசயம்.
எனது ஆராய்ச்சியை பற்றி எழுதும்போது இது குறித்து மிக விளக்கமாக எழுதுகிறேன். ஏனெனில் நான் முதன்முதலில் எடு்த்துக்கொண்ட ஆராய்ச்சியும் இப்போது செய்து வரும் ஆராய்ச்சிக்கும் அதிக தொடர்பு உண்டு.
மின்பகுப்பு முறையானது சில தனிமங்களை பிரித்தெடுக்க உதவுகிறது. பொதுவாக மின்பகுப்பு முறையில் புரட்டான்களும், எலக்ட்ரான்களும் சுதந்திரமாக வலம் வர வேண்டும். அப்படியில்லாதபட்சத்தில் பிரித்தெடுப்பது என்பது இயலாத ஒன்று.
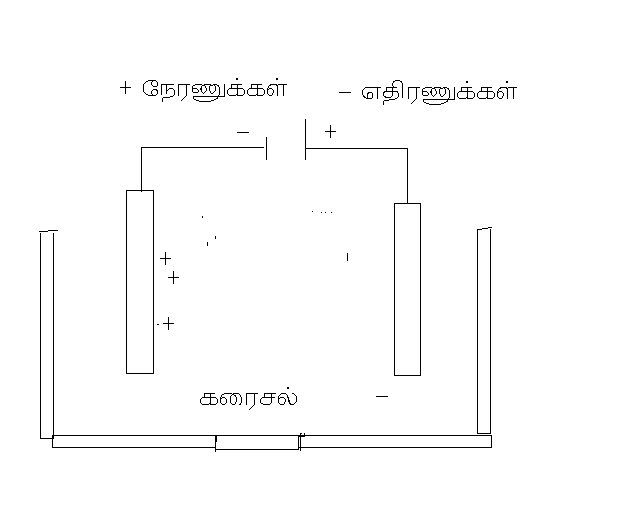
மின்பகுப்பு முறைக்கு உட்படுத்தப்படும் தனிமம் எலக்ட்ரான்களை இழக்க தயாராக இருக்க வேண்டும். நேரணுக்கள், எதிரணுக்கள் அவசியம். அதைப்போல நேரணுக்களைப் பெற எதிர் மின்கடத்தி, எதிரணுக்களைப் பெற நேர் மின்கடத்தி அவசியமாகிறது.
மின்சாரத்தைப் பாய்ச்சும்போது தனிமமானது தன்னிலை இழக்க வேண்டும். பொதுவாக தண்ணீரில் அந்த பொருளை கரைத்து இருக்க வேண்டும் அல்லது உருகிய நிலையில் இருக்க வேண்டும். திடப்பொருளாக இருக்கும்பட்சத்தில் எலக்ட்ரான்கள் சுதந்திரமாக இருப்பது கடினமாகும்.
உதாரணத்திற்கு அலுமினியம் எடுத்துக்கொள்வோம். இது பாக்ஸைட்டாக கிடைக்கிறது. அதாவது அலுமினியம் ஆக்ஸைடாக பூமியிலிருந்து கிடைக்கிறது. இதில் அலுமினியம் நேரணுக்கள் கொண்டது. ஆக்ஸிஜன் எதிரணுக்கள் கொண்டது. இந்த பாக்ஸைடிலிருந்து அலுமினியத்தை பிரிக்க அப்படியே உபயோகிக்க இயலாது, காரணம் வெப்பநிலை மிகவும் அதிகமாகும். மேலும் இந்த பாக்ஸைட்டுடன் வேறு சில பொருட்கள் கலந்து இருக்கும். அவைகளை கரைத்தல் முறை மூலம் நீக்கலாம். பாக்ஸைட்டை பிற கலப்பட பொருட்களிலிருந்து நீக்கிவிட்டு அதனுடன் கிரையோலைட் எனப்படும் பொருளை கலக்க வேண்டும். இப்போது பாக்ஸைட் 900 டிகிரியிலே உருக ஆரம்பிக்கும். இதற்கு முன்னர் 2000 டிகிரி வேண்டும்.
இந்த நிலையை அடைந்தவுடன் இதனை மின்பகுப்பு பானையில் போட்டு மின்கடத்திகளை இணைக்க வேண்டும். மின்சாரம் பாய்ச்சியவுடன் பாக்ஸைடிலிருந்து அலுமினியம் நேர் சக்தியுடனும், ஆக்ஸிஜன் எதிர் சக்தியுடனும் பிரிகிறது அவ்வாறு பிரிந்து நேர் சக்தி எதிர் மின் கடத்திக்கும், எதிர் சக்தி நேர் மின் கடத்திக்கும் செல்கிறது. கார்பன் மின்கடத்தியாக உபயோகிக்கப்படுகிறது. ஆக்ஸிஜன் கார்பனுடன் சேர்ந்து கரியமில வாயுவாக மாறிவிடுவதால் அந்த மின்கடத்தியை அடிக்கடி மாற்றுவது அவசியமாகும். இவ்வாறு அலுமினியம் பிரித்தெடுக்கப்படுகிறது.
மின்பகுப்பு முறைக்கு உட்படுத்தப்படும் தனிமம் எலக்ட்ரான்களை இழக்க தயாராக இருக்க வேண்டும். நேரணுக்கள், எதிரணுக்கள் அவசியம். அதைப்போல நேரணுக்களைப் பெற எதிர் மின்கடத்தி, எதிரணுக்களைப் பெற நேர் மின்கடத்தி அவசியமாகிறது.
மின்சாரத்தைப் பாய்ச்சும்போது தனிமமானது தன்னிலை இழக்க வேண்டும். பொதுவாக தண்ணீரில் அந்த பொருளை கரைத்து இருக்க வேண்டும் அல்லது உருகிய நிலையில் இருக்க வேண்டும். திடப்பொருளாக இருக்கும்பட்சத்தில் எலக்ட்ரான்கள் சுதந்திரமாக இருப்பது கடினமாகும்.
உதாரணத்திற்கு அலுமினியம் எடுத்துக்கொள்வோம். இது பாக்ஸைட்டாக கிடைக்கிறது. அதாவது அலுமினியம் ஆக்ஸைடாக பூமியிலிருந்து கிடைக்கிறது. இதில் அலுமினியம் நேரணுக்கள் கொண்டது. ஆக்ஸிஜன் எதிரணுக்கள் கொண்டது. இந்த பாக்ஸைடிலிருந்து அலுமினியத்தை பிரிக்க அப்படியே உபயோகிக்க இயலாது, காரணம் வெப்பநிலை மிகவும் அதிகமாகும். மேலும் இந்த பாக்ஸைட்டுடன் வேறு சில பொருட்கள் கலந்து இருக்கும். அவைகளை கரைத்தல் முறை மூலம் நீக்கலாம். பாக்ஸைட்டை பிற கலப்பட பொருட்களிலிருந்து நீக்கிவிட்டு அதனுடன் கிரையோலைட் எனப்படும் பொருளை கலக்க வேண்டும். இப்போது பாக்ஸைட் 900 டிகிரியிலே உருக ஆரம்பிக்கும். இதற்கு முன்னர் 2000 டிகிரி வேண்டும்.
இந்த நிலையை அடைந்தவுடன் இதனை மின்பகுப்பு பானையில் போட்டு மின்கடத்திகளை இணைக்க வேண்டும். மின்சாரம் பாய்ச்சியவுடன் பாக்ஸைடிலிருந்து அலுமினியம் நேர் சக்தியுடனும், ஆக்ஸிஜன் எதிர் சக்தியுடனும் பிரிகிறது அவ்வாறு பிரிந்து நேர் சக்தி எதிர் மின் கடத்திக்கும், எதிர் சக்தி நேர் மின் கடத்திக்கும் செல்கிறது. கார்பன் மின்கடத்தியாக உபயோகிக்கப்படுகிறது. ஆக்ஸிஜன் கார்பனுடன் சேர்ந்து கரியமில வாயுவாக மாறிவிடுவதால் அந்த மின்கடத்தியை அடிக்கடி மாற்றுவது அவசியமாகும். இவ்வாறு அலுமினியம் பிரித்தெடுக்கப்படுகிறது.
ஒரு வேதியியல் வினை என்பது அத்தனை எளிதான விசயமல்ல என்பதை மீண்டும் நிரூபிக்கும் முறையாக சில வேதியியல் வினைகளை மேற்கொண்டதில் அறிந்து கொள்ள முடிந்தது. இந்த வேதிவினையை சில காரணங்களால் இங்கு எழுதி விளக்கமுடியாத நிலை. இந்த ஒருங்கிணைந்த மூலக்கூறுகள் மருந்துகளாக மாறக்கூடிய வாய்ப்பு இருப்பதால் இவைகளை இப்போது மறைத்து வைக்க வேண்டிய கட்டாயம்.
வேதியியல் வினைக்கு வருவோம்.
1. இரண்டு வெவ்வேறு தொடக்க மூலக்கூறுகள். சிறு மாற்றம் மட்டுமே ஒரு மூலக்கூறுக்கும் மற்றொரு மூலக்கூறுக்கும்.
2. இந்த இரண்டு மூலக்கூறும் வினைபுரியக்கூடிய காரணிகள் ஒன்றுதான். அந்த காரணிகளில் எந்த மாற்றமுமில்லை.
3. எல்லா சூழலும் ஒன்றாக இருக்க ஒரு மூலக்கூறு மட்டுமே நினைத்தபடி வினைபுரிந்தது, மற்றொரு மூலக்கூறு வேறு விதமாக வினைபுரிந்தது.
இப்படி சிறு மாற்றங்களே கொண்ட மூலக்கூறு வினைபுரியும் தன்மை மட்டும் வேறுபாடன்றி, நமது உடலில் அவை செயல்படும் முறையும் வித்தியாசமாக இருப்பது வியப்புக்குரியதுதான்.
மேலும் இப்பொழுதெல்லாம் தொழில் நுட்ப முன்னேற்றத்தால், முன்னர் போல் இந்த வியாதிக்கு இந்த மூலக்கூறு சரியாக இருக்கும் என உட்கார்ந்து யோசிக்க வேண்டியதெல்லாம் இல்லை. கணினியில், வியாதிக்கு காரணமான ரிசெப்டார் (receptor) எதுவென கொடுத்தால் அந்த ரிசெப்டாரில் சென்று உட்காரும் மூலக்கூறுகள் என பல மூலக்கூறுகளை தந்துவிடுகிறது. ஆனாலும் ஒரு மருந்தை உருவாக்குவது என்பது இன்னும் அத்தனை எளிதான காரியமாகவே இல்லை! விரைவில் அதற்கான வழியை கண்டுபிடிப்போம்.
வேதியியல் வினைக்கு வருவோம்.
1. இரண்டு வெவ்வேறு தொடக்க மூலக்கூறுகள். சிறு மாற்றம் மட்டுமே ஒரு மூலக்கூறுக்கும் மற்றொரு மூலக்கூறுக்கும்.
2. இந்த இரண்டு மூலக்கூறும் வினைபுரியக்கூடிய காரணிகள் ஒன்றுதான். அந்த காரணிகளில் எந்த மாற்றமுமில்லை.
3. எல்லா சூழலும் ஒன்றாக இருக்க ஒரு மூலக்கூறு மட்டுமே நினைத்தபடி வினைபுரிந்தது, மற்றொரு மூலக்கூறு வேறு விதமாக வினைபுரிந்தது.
இப்படி சிறு மாற்றங்களே கொண்ட மூலக்கூறு வினைபுரியும் தன்மை மட்டும் வேறுபாடன்றி, நமது உடலில் அவை செயல்படும் முறையும் வித்தியாசமாக இருப்பது வியப்புக்குரியதுதான்.
மேலும் இப்பொழுதெல்லாம் தொழில் நுட்ப முன்னேற்றத்தால், முன்னர் போல் இந்த வியாதிக்கு இந்த மூலக்கூறு சரியாக இருக்கும் என உட்கார்ந்து யோசிக்க வேண்டியதெல்லாம் இல்லை. கணினியில், வியாதிக்கு காரணமான ரிசெப்டார் (receptor) எதுவென கொடுத்தால் அந்த ரிசெப்டாரில் சென்று உட்காரும் மூலக்கூறுகள் என பல மூலக்கூறுகளை தந்துவிடுகிறது. ஆனாலும் ஒரு மருந்தை உருவாக்குவது என்பது இன்னும் அத்தனை எளிதான காரியமாகவே இல்லை! விரைவில் அதற்கான வழியை கண்டுபிடிப்போம்.
வேதியியலை விளங்கிக் கொள்ளவே முடிவதில்லை. சில நேரங்களில் மிகவும் மனதை தளர்வடையச் செய்துவிடும். ஒரு ஒருங்கிணைந்த மூலக்கூறினை உருவாக்கிவிட்டோம் என இறுமாந்து இருந்துவிடமுடியாதுதான். ஒரு ஒருங்கிணைந்த மூலக்கூறினை உருவாக்கி அந்த மூலக்கூறு சரிதானா என ஆதாரத்துடன் காண்பிக்க வேண்டும்.
நிறை மட்டும் எத்தனை புரோட்டான் உள்ளது என ஆராய வேண்டும். அவை சரியாக இருந்தால் ஓரளவு நம்பிக்கை கொள்ளலாம். ஆனால் அதற்கு மேலாக அந்த மூலக்கூறில் கார்பன், ஹைட்ரஜன், நைட்ரஜன், குளோரின் என அனைத்தும் சரியான விகிதத்தில் அமைந்திருக்க வேண்டும். இவை சரியாக அமைந்திருந்தால் மட்டுமே அந்த மூலக்கூறு மிகவும் தூய்மையான ஒன்றாக கருத முடியும்.
இப்படி ஒருமுறை ஒரு மூலக்கூறினை உருவாக்கி ஆராய்ந்தபோது சம்பந்தமே இல்லாமல் இருந்தது. செய்முறை எல்லாம் சரி செய்து பார்த்தபின்னரும் இந்த விசயம் ஆச்சரியமாக இருந்தது. இந்த பணியை செய்தவரிடம் கேட்டபொழுது அவர்களும் மிகச்சரியே, மூலக்கூறில் தான் பிரச்சினை என்றார்கள்.
சில நாட்கள் பின்னர் அதே மூலக்கூறினை அனுப்பியபோது மிகச் சரியான விகிதத்தில் இருந்தது. நான் முதலில் அனுப்பியதுதான் என்ன என கண்டுபிடிக்கவே இயலவில்லை. அவர்கள் தவறு செய்யவில்லை எனவும் சொல்லிவிட்டார்கள்.
ஒரு ஒருங்கிணைந்த மூலக்கூறு உருவாக்குவது என்பது இந்த பணியில் இருப்போர்க்கு மிகவும் எளிதாக இருக்கக்கூடும். சில வேளைகளில் மிகவும் கடினமானதாகவே இருக்கிறது.
முன்னர் சொன்னதுபோல இத்தனை சிரமம் பட்டு செய்தாலும் பல்லாயிரம் மூலக்கூறுகளில் ஒரு மூலக்கூறு மட்டுமே நாம் எதிர்பார்க்கும் பலன் தருகிறது என்பது மருத்துவ உலகிற்கு தொடர்ந்து ஏற்பட்டு வரும் போராட்டம் தான்.
நிறை மட்டும் எத்தனை புரோட்டான் உள்ளது என ஆராய வேண்டும். அவை சரியாக இருந்தால் ஓரளவு நம்பிக்கை கொள்ளலாம். ஆனால் அதற்கு மேலாக அந்த மூலக்கூறில் கார்பன், ஹைட்ரஜன், நைட்ரஜன், குளோரின் என அனைத்தும் சரியான விகிதத்தில் அமைந்திருக்க வேண்டும். இவை சரியாக அமைந்திருந்தால் மட்டுமே அந்த மூலக்கூறு மிகவும் தூய்மையான ஒன்றாக கருத முடியும்.
இப்படி ஒருமுறை ஒரு மூலக்கூறினை உருவாக்கி ஆராய்ந்தபோது சம்பந்தமே இல்லாமல் இருந்தது. செய்முறை எல்லாம் சரி செய்து பார்த்தபின்னரும் இந்த விசயம் ஆச்சரியமாக இருந்தது. இந்த பணியை செய்தவரிடம் கேட்டபொழுது அவர்களும் மிகச்சரியே, மூலக்கூறில் தான் பிரச்சினை என்றார்கள்.
சில நாட்கள் பின்னர் அதே மூலக்கூறினை அனுப்பியபோது மிகச் சரியான விகிதத்தில் இருந்தது. நான் முதலில் அனுப்பியதுதான் என்ன என கண்டுபிடிக்கவே இயலவில்லை. அவர்கள் தவறு செய்யவில்லை எனவும் சொல்லிவிட்டார்கள்.
ஒரு ஒருங்கிணைந்த மூலக்கூறு உருவாக்குவது என்பது இந்த பணியில் இருப்போர்க்கு மிகவும் எளிதாக இருக்கக்கூடும். சில வேளைகளில் மிகவும் கடினமானதாகவே இருக்கிறது.
முன்னர் சொன்னதுபோல இத்தனை சிரமம் பட்டு செய்தாலும் பல்லாயிரம் மூலக்கூறுகளில் ஒரு மூலக்கூறு மட்டுமே நாம் எதிர்பார்க்கும் பலன் தருகிறது என்பது மருத்துவ உலகிற்கு தொடர்ந்து ஏற்பட்டு வரும் போராட்டம் தான்.
ஒரு மருந்தைக் கண்டுபிடிப்பது குறித்து ஆய்வகம் இல்லாத அந்த காலத்தில் என்ன முறையைக் கண்டுபிடித்தார்கள் எனத் தெரியவைல்லை. ஆனால் கண்டுபிடிக்கப்பட்ட மருந்துகள் உண்மையிலேயே நோய் தீர்க்கும் மருந்தாக இருந்ததுதான் மிகவும் ஆச்சரியம். முன்னோர்கள் சொன்னது என்றே வைத்துக்கொள்வோம், முன்னோர்களுக்கு யார் சொன்னது என கேள்வி வந்து சேரும். தேடித் தேடி அலுத்துப் போயிருப்பார்கள் தான்.
ஆய்வகம் இல்லாத சூழ்நிலையினால் மொத்தமாக சாற்றினைப் பிழிந்து அப்படியே உபயோகித்த வழக்கம்தான் இருந்து வந்தது. அதுவும் ஒன்றை மட்டும் தராமல் பிற செடி இனங்களையும் அரைத்து தரும் வழக்கம் இருந்தது. இப்படி ஒன்றோடு ஒன்று இணைவதால் என்ன விளைவுகள் வந்தது, என்ன நேர்ந்தது என எவரேனும் ஒருவேளை எழுதி இருக்கலாம். மருத்துவம் எழுதிய நமது போகர் சித்தர் போல. போகர் சித்தர் எழுதியதாக நான் கேள்விபட்டதுதான் உண்டு. ஆனால் இதுவரை அவர் எழுதியதைப் படித்தது கூட இல்லை என்பதே உண்மையான விசயமாகும்.
நாளடைவில் பாட்டி வைத்தியம் என சொல்லும் அளவிற்கு மிகவும் பிரசித்தி பெற்று இருந்தது இந்த வைத்திய முறைகள். அதுவும் தலை வலித்தால் என்ன பண்ணுவார்களாம் எனில், தலையில் பக்கவாட்டில் ஒரு ஓட்டை போடுவார்களாம். இதுதான் அறுவை சிகிச்சைக்கான முதல் படி. ஏதாவது வெட்டு பட்டால் அதை சுற்றி இலைகள் வைத்துக் கட்டுபோடுவதுதான் வழக்கமாக இருந்தது. மாவுக் கட்டு தெரியாத கிராமவாசி இருக்க முடியாது. பின்னர் உடலைக் கூறுபோட்டு என்ன இருக்கிறது எனப் பார்க்கத் தொடங்கிய காலமும் உண்டு.
இப்படி மொத்த மருத்துவமும் உள்ள செடியை முதன்முதலாகப் பிரித்து எடுத்துப் பார்க்க ஆசை வந்தது. எப்படி மருந்து உருவானது என்பது ஒரு பெரிய கதைதான். இப்படி செடிகள் தரும் மருந்து என்ன என நினைத்தபோதுதான் ஒரு எண்ணம் உதயமானது.
அந்த செடியை காயவைத்தார்கள். பொடியாக்கினார்கள். தண்ணீரிலும் பிற ரசாயனங்களிலும் மூழ்க வைத்தார்கள். இந்த முறைதான் ஒரு மூலக்கூறினைப் பிரித்தெடுக்க வைத்த வழியாகும்.
ஆய்வகம் இல்லாத சூழ்நிலையினால் மொத்தமாக சாற்றினைப் பிழிந்து அப்படியே உபயோகித்த வழக்கம்தான் இருந்து வந்தது. அதுவும் ஒன்றை மட்டும் தராமல் பிற செடி இனங்களையும் அரைத்து தரும் வழக்கம் இருந்தது. இப்படி ஒன்றோடு ஒன்று இணைவதால் என்ன விளைவுகள் வந்தது, என்ன நேர்ந்தது என எவரேனும் ஒருவேளை எழுதி இருக்கலாம். மருத்துவம் எழுதிய நமது போகர் சித்தர் போல. போகர் சித்தர் எழுதியதாக நான் கேள்விபட்டதுதான் உண்டு. ஆனால் இதுவரை அவர் எழுதியதைப் படித்தது கூட இல்லை என்பதே உண்மையான விசயமாகும்.
நாளடைவில் பாட்டி வைத்தியம் என சொல்லும் அளவிற்கு மிகவும் பிரசித்தி பெற்று இருந்தது இந்த வைத்திய முறைகள். அதுவும் தலை வலித்தால் என்ன பண்ணுவார்களாம் எனில், தலையில் பக்கவாட்டில் ஒரு ஓட்டை போடுவார்களாம். இதுதான் அறுவை சிகிச்சைக்கான முதல் படி. ஏதாவது வெட்டு பட்டால் அதை சுற்றி இலைகள் வைத்துக் கட்டுபோடுவதுதான் வழக்கமாக இருந்தது. மாவுக் கட்டு தெரியாத கிராமவாசி இருக்க முடியாது. பின்னர் உடலைக் கூறுபோட்டு என்ன இருக்கிறது எனப் பார்க்கத் தொடங்கிய காலமும் உண்டு.
இப்படி மொத்த மருத்துவமும் உள்ள செடியை முதன்முதலாகப் பிரித்து எடுத்துப் பார்க்க ஆசை வந்தது. எப்படி மருந்து உருவானது என்பது ஒரு பெரிய கதைதான். இப்படி செடிகள் தரும் மருந்து என்ன என நினைத்தபோதுதான் ஒரு எண்ணம் உதயமானது.
அந்த செடியை காயவைத்தார்கள். பொடியாக்கினார்கள். தண்ணீரிலும் பிற ரசாயனங்களிலும் மூழ்க வைத்தார்கள். இந்த முறைதான் ஒரு மூலக்கூறினைப் பிரித்தெடுக்க வைத்த வழியாகும்.